Intercambios de Trabajo y Calor
El estudio del trabajo y el calor es fundamental dentro de la termodinámica, ya que ambos representan formas de transferencia de energía entre sistemas físicos. Cuando se realiza trabajo mecánico sobre un cuerpo, parte de esa energía puede convertirse en calor, lo que produce un aumento en la temperatura del sistema. Este principio fue analizado con profundidad por James Prescott Joule, quien demostró experimentalmente que el trabajo y el calor son equivalentes y pueden transformarse mutuamente. Su famoso experimento con paletas agitadoras permitió establecer el equivalente mecánico del calor, que indica cuánta energía mecánica se requiere para producir una cantidad específica de calor. Gracias a sus mediciones, se determinó que 1 caloría corresponde aproximadamente a 4,186 joules.
A partir de estas ideas surge el primer principio de la termodinámica, también conocido como principio de conservación de la energía. Este establece que el cambio en la energía interna de un sistema es igual al calor que recibe menos el trabajo que realiza, expresado matemáticamente como:
Este principio afirma que la energía no se crea ni se destruye, solo se transforma.
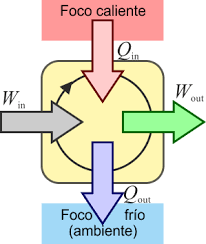
Finalmente, el proceso inverso - la conversión de calor en trabajo - se observa en las máquinas térmicas. Estos dispositivos reciben calor de una fuente caliente, transforman parte de esa energía en trabajo útil y expulsan el resto a un foco frío. Su eficiencia depende del diseño y de las condiciones del ciclo térmico que emplean, siendo el ciclo de Carnot el modelo teórico más eficiente.