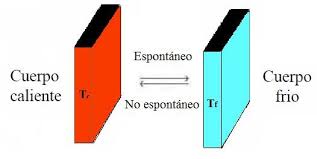
ESPOSTANEIDAD Y PROCESOS TERMODINÁMICOS
La espontaneidad en termodinámica se refiere a la capacidad que tiene un proceso para ocurrir sin la necesidad de un trabajo externo. Un proceso espontáneo no siempre es rápido, pero sí tiene una tendencia natural a suceder. Por ejemplo, el calor fluye espontáneamente de un cuerpo caliente a uno frío, y los gases se expanden hasta ocupar todo el recipiente disponible. Estos procesos ocurren porque llevan al sistema y al entorno hacia un estado más probable y disperso.
La entropía (S) es una magnitud que mide el grado de desorden o dispersión de la energía en un sistema. Cuanto mayor es el desorden, mayor es la entropía. Los sólidos poseen baja entropía, los líquidos tienen un valor intermedio y los gases presentan valores altos debido a la libertad de movimiento de sus partículas. En términos energéticos, la entropía también indica cómo se distribuye la energía disponible dentro de un sistema.
El segundo principio de la termodinámica establece que la entropía total del universo siempre tiende a aumentar en cualquier proceso espontáneo. Esto implica que la energía útil se degrada con el tiempo y que no es posible regresar un sistema exactamente a su estado inicial sin gastar energía adicional. Las máquinas térmicas, por ejemplo, nunca pueden convertir todo el calor en trabajo, ya que parte de la energía siempre se dispersa y aumenta la entropía.
En conclusión, la espontaneidad, la entropía y el segundo principio están estrechamente relacionados, pues describen la tendencia natural de los sistemas a evolucionar hacia estados más desordenados y estables.